Retrotranscriptasa del virus de la inmunodeficiencia humana y terapia antirretroviral
Resumen de Investigación:
A pesar de los éxitos de la terapia antirretroviral, las infecciones causadas por los virus de la inmunodeficiencia humana de tipo 1 y 2 (VIH-1 y VIH-2, respectivamente) son responsables de 1,6 millones de muertes cada año. La retrotranscriptasa (RT) del VIH juega un papel clave en la replicación del ARN genómico vírico y sus inhibidores constituyen la base de los tratamientos más utilizados y eficaces.
Desde hace años, nuestros esfuerzos se han dirigido hacia la determinación de mecanismos moleculares implicados en resistencia a inhibidores de la RT y conocer el papel que juegan distintos aminoácidos en su especificidad de nucleótido y fidelidad de copia. A lo largo de nuestras investigaciones hemos obtenido RTs del VIH-1 que presentan elevada estabilidad térmica y/o fidelidad de síntesis de ADN. Algunas de estas RTs son comercializadas en la actualidad y se usan en distintas aplicaciones biotecnológicas tanto en investigación básica como clínica. Objetivos futuros incluyen el desarrollo de nuevas RTs con elevada afinidad por ácidos nucleicos que pudieran ser útiles en amplificación de ARN a partir de células individuales.
Aunque los análogos a nucleósido constituyen la base de las terapias actuales frente al VIH, las mutaciones asociadas con resistencia a estos inhibidores son diferentes en el VIH-1 y en el VIH-2. Recientemente hemos demostrado que la presencia de Met-73 e Ile-75 en la RT del VIH-2 impide el desarrollo de resistencia a través del mecanismo de escisión, justificando por qué las mutaciones de resistencia a análogos a timidina (M41L, D67N, K70R o T215Y) son raras en los pacientes infectados por el VIH-2 y sometidos a tratamiento antirretroviral.
Actualmente, la prevalencia de mutaciones de resistencia está aumentando en los países menos desarrollados, lo que hace pensar que se necesitarán nuevos fármacos antirretrovirales que exploten otras dianas del ciclo replicativo del VIH. En este sentido, también estamos interesados en la actividad ribonucleasa H de la RT, y en identificar factores del hospedador que pudieran comprometer la eficacia replicativa del VIH.
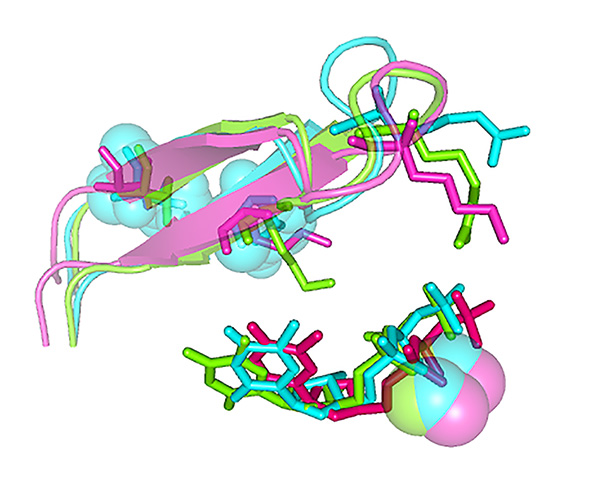
Superposición de modelos moleculares de complejos ternarios constituidos por la RT silvestre del VIH-1 o los mutantes D67N/K70R y D67N/K70R/K73M, unidos a ADN de doble cadena y un nucleótido entrante. Se muestra la horquilla β3-β4, el dNTP entrante y los dos Mg2+ del centro catalítico, para resaltar la influencia de Met-73 en la interacción de Arg-70 con el dNTP entrante. Para más detalles, véase el trabajo de Álvarez et al. (2018) J. Biol. Chem., 293, 2247-2259.
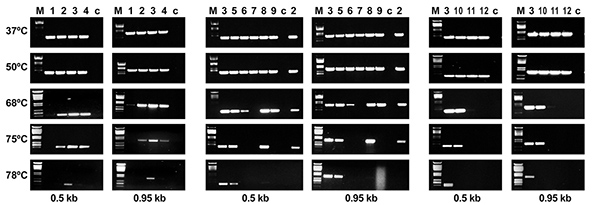
Ensayos de RT-PCR en los que se muestra el efecto de la temperatura sobre la síntesis de cDNA catalizada por distintas variantes de la RT del VIH-1 grupo O (Matamoros et al. 2013; Biochemistry 52, 9318).

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Caz Calvo | Rubén del | 124 | 4523 | Estudiante TFM | |
| Estévez Barcia | Rebeca | 124 | 4523 | Estudiante TFG | |
| Martínez del Río | Javier | 124 | 4523 | javier.martinez(at)cbm.csic.es | Titulado Sup. Actividades Tecn. y Prof.GP1 |
| Menéndez Arias | Luis | 124 | 4494 | lmenendez(at)cbm.csic.es | E. Profesores de Investigación de Organismos Públicos de Investigación |
| Rello García | Nuria | 124 | 4494/4523 | Estudiante TFM |
Publicaciones relevantes:
- Menéndez-Arias, L. (2013) Molecular basis of human immunodeficiency virus type 1 drug resistance: Overview and recent developments. Antiviral Res. 98, 93-120; doi:10.1016/j.an-tiviral.2013.01.007.
- Álvarez, M., Barrioluengo, V., Afonso-Lehmann, R.N., Menéndez-Arias, L. (2013) Altered error specificity of RNase H-deficient HIV-1 reverse transcriptases during DNA-dependent DNA synthesis. Nucleic Acids Res. 41, 4601-4612; doi:10.1093/nar/gkt109.
- Matamoros, T., Barrioluengo, V., Abia, D., Menéndez-Arias, L. (2013) Major groove binding track residues of the connection subdomain of human immunodeficiency virus type 1 reverse transcriptase enhance cDNA synthesis at high temperatures. Biochemistry 52, 9318-9328; doi:10.1021/bi401390x.
- Betancor, G., Álvarez, M., Marcelli, B., Andrés, C., Martínez, M.A., Menéndez-Arias, L. (2015) Effects of HIV-1 reverse transcriptase connection subdomain mutations on polypurine tract removal and initiation of (+)-strand DNA synthesis. Nucleic Acids Res. 43, 2259-2270.
- Álvarez, M., Sebastián-Martín, A., García-Marquina, G., Menéndez-Arias, L. (2017) Fidelity of classwide-resistant HIV-2 reverse transcriptase and differential contribution of K65R to the accuracy of HIV-1 and HIV-2 reverse transcriptases. Sci. Rep. 7, 44834. doi:10.1038/srep44834.
- Álvarez, M., Nevot, M., Mendieta, J., Martínez, M.A., Menéndez-Arias, L. (2018) Amino acid residues in HIV-2 reverse transcriptase that restrict the development of nucleoside analogue resistance through the excision pathway. J. Biol. Chem. 293, 2247-2259; doi:10.1074/jbc.RA117.000177.
- Sebastián-Martín, A., Barrioluengo, V., Menéndez-Arias, L. (2018) Transcriptional inaccuracy threshold attenuates differences in RNA-dependent DNA synthesis fidelity between retroviral reverse transcriptases. Sci. Rep. 8, 627; doi:10.1038/s41598-017-18974-8.
- Sun, L., Gao, P., Dong, G., Zhang, X., Cheng, X., Ding, X., Wang, X., Daelemans, D., De Clercq, E., Pannecouque, C., Menéndez-Arias, L., Zhan, P., Liu, X. (2018) 5-Hydroxypyrido[2,3-b]pyrazin-6(5H)-one derivatives as novel dual inhibitors of HIV-1 reverse transcriptase-associated ribonuclease H and integrase. Eur. J. Med. Chem. 155, 714-724; doi:10.1016/j.ejmech.2018.06.036.
- Luczkowiak, J., Matamoros, T., Menéndez-Arias, L. (2018) Template-primer binding affinity and RNase H cleavage specificity contribute to the strand transfer efficiency of HIV-1 reverse transcriptase. J. Biol. Chem. 293, 13351-13363; doi:10.1074/jbc.RA118.004324.
- Tramontano, E., Corona, A., Menéndez-Arias, L. (2019) Ribonuclease H, an unexploited target for antiviral intervention against HIV and hepatitis B virus. Antiviral Res. 171, 104613; doi: 10.1016/j.antiviral.2019.104613.




















